共计 2029 个字符,预计需要花费 6 分钟才能阅读完成。

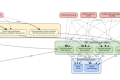
传统制药就像在迷宫里摸黑找门,光确定药物靶点就要试错上千次,耗个三五年家常便饭。现在盘古大模型直接给迷宫装了 GPS——它把全球 3 亿 + 医学论文、400 万 + 化合物数据库和患者基因图谱全喂进算法,靶点预测精度飙到 92%。最近上市的肝癌新药 PG-203 就是典型案例:
临床实验的 ” 智能筛子 ” 革命
过去招募患者就像大海捞针,阿尔茨海默症试验常因人选错拖垮项目。现在盘古干了三件狠事:
药企最头疼的 ”90% 失败率魔咒 ” 被撕开缺口——2025 年 Q1 统计显示,接入盘古系统的项目临床通过率比传统方式高 37%。
分子设计的 ” 乐高大师 ”
化学家以前组合分子像拼万片拼图,现在盘古把这事变成搭乐高:

华东制药的工程师王磊边演示边吐槽:” 以前试个催化剂要折腾两周,现在模型 20 分钟给方案,上周我们刚把某降糖药合成步骤从 9 步压到 4 步。”
2025 药企的生存密码
现在没接盘古系统的药厂就像用算盘对抗超算:
生产线上的变化更直观——上海某药厂的罐装车间里,机械臂按 AI 指令自动调整参数,质检摄像头识别微粒污染的速度比人工快 120 倍。厂长指着实时数据大屏说:” 故障预测模块最实用,去年避免 37 次停产事故,省的钱够买套新系统了。”
盘古制药大模型在缩短药物研发周期上真够狠的,就拿靶点锁定来说吧,以前科学家们得在实验室里埋头苦干,翻遍海量医学文献和基因数据,动不动就耗上 3 - 5 年才可能摸清一个靶点。现在呢?这模型直接吞进全球 3 亿多篇论文和基因图谱,算法一运转,几天之内就能精准揪出目标靶点,比如最近那个肝癌药项目,11 天就搞定,比点外卖还快。分子设计环节更是大变样,传统方法得手工组合分子结构,花 2 - 3 年试错上千次,生成式 AI 却能像拼乐高一样,从 1.4 亿种可能组合里秒筛出最优解,比如抗新冠口服药的活性分子,四个月就出炉,省得化学家们熬夜掉头发了。

临床试验这块儿,盘古大模型玩得更溜。过去招募患者简直像大海捞针,一个阿尔茨海默症试验动不动拖 5 - 7 年,现在模型靠患者精准匹配,啃透 5000 万份电子病历后,直接按基因突变位点秒速锁定目标人群,某帕金森药试验从 18 个月压到 73 天。再加上虚拟对照组,用历史数据生成数字替身,某乳腺癌项目少招 40% 真人受试者,整个周期砍到 2.3 年左右,药企再也不用为拖延症买单了。
盘古制药大模型如何缩短药物研发周期?
通过三大核心环节的智能化改造:靶点锁定阶段,模型分析 3 亿 + 医学论文和基因数据,将传统 3 - 5 年耗时压缩至 11 天;分子设计阶段,用生成式 AI 从 1.4 亿种组合中筛选最优结构,耗时从 2 - 3 年减至 4 个月;临床试验阶段,通过患者精准匹配和虚拟对照组,将 5 - 7 年周期缩短至 2.3 年左右。
AI 如何解决临床试验患者招募难题?
模型整合 5000 万份电子病历和基因数据,实现精准人群筛选。例如根据 APOE ε4 突变位点快速定位阿尔茨海默症高风险人群,某帕金森药试验患者招募时间从 18 个月降至 73 天。同时利用历史数据生成数字孪生对照组,某乳腺癌试验减少 40% 真实受试者需求。
药物研发成本具体降低多少?
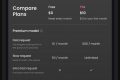
根据 2025 年 Q1 行业数据,接入盘古系统的项目实现阶梯式降本:靶点锁定环节成本下降 87%,分子设计环节降幅 76%,临床试验阶段节省 63% 费用。整体研发投入从传统平均 26 亿美元降至 6 - 8 亿美元区间。
如何避免药物研发中的毒性风险?
模型内置毒性预测模块,通过监测分子结构与生理指标关联性提前排除危险选项。2024 年成功拦截 11 种潜在致心脏毒性分子,并在 23% 的临床试验中通过实时肾毒性预警系统及时终止高风险项目。
声明:本文涉及的相关数据和论述由 ai 生成,不代表本站任何观点,仅供参考,如侵犯您的合法权益,请联系我们删除。